Ancol Anlylic là một trong những hợp chất quan trọng có trong chương trình Hóa học phổ thông. Một số kiến thức liên quan đến hợp chất này sẽ được lồng ghép vào trong các đề thi. Vì vậy, để giúp các em chinh phục các dạng bài về Ancol Anlylic, Marathon Education sẽ tổng hợp những kiến thức trọng tâm cũng như bài tập vận dụng qua bài viết dưới đây.
Ancol Anlylic là gì?
Ancol Anlylic là một hợp chất hữu cơ có công thức hóa học là C3H5OH hay C3H6O. Hợp chất này khá nguy hiểm, có độc tính nên thường được ứng dụng để sản xuất thuốc trừ sâu và các chất hữu cơ khác.
Công thức cấu tạo của Ancol Anlylic
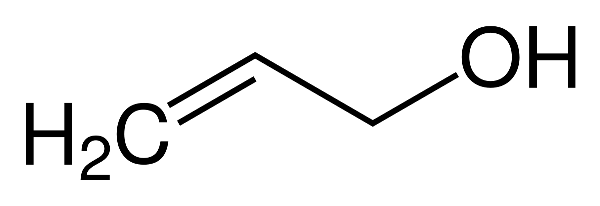
Ancol Anlylic có công thức cấu tạo là CH2=CH-CH2-OH.
Tên gọi khác
Dựa theo quy ước quốc tế IUPAC, Ancol Anlylic còn có tên thay thế là 2-Propen-1-ol. Ngoài ra, tên gọi thông thường của Ancol Anlylic được nhiều người biết đến là rượu anlylic.
Tính chất đặc trưng của Ancol Anlylic
Để hiểu rõ hơn về rượu anlylic, các em cần phải nắm vững các tính chất đặc trưng như sau:
- Ancol Anlylic là một chất lỏng không màu. Ở nồng độ cao, hợp chất có mùi mù tạc. Ở nồng độ thấp hơn, hợp chất sẽ có mùi tương tự như etanol.
- Điểm sôi: 97°C.
- Điểm nóng chảy: -129°C.
Điều chế Ancol Anlylic
Có 4 phương pháp chính để điều chế Ancol Anlylic:
- Khử nước propan – 1 – ol.
- Thủy phân propen chloride.
- Oxy hóa propylen oxide và kali alum (KAl(SO4)2•12H2O) ở nhiệt độ cao.
- Cho glycerol tác dụng với acid formic.
Bài tập vận dụng
Để các em có thể ghi nhớ tốt hơn phần kiến thức về Ancol Anlylic, hãy cùng Team Marathon Education điểm qua một số dạng bài tập vận dụng thường gặp dưới đây.
Bài 1: Cho hỗn hợp X gồm etanol, propan-1-ol và ancol anlylic và chia đều hỗn hợp thành 3 phần bằng nhau. Khi đem phần 1 cho tác dụng với Na dư thì thu được 1,68 lít H2 (đktc). Phần 2 có khả năng làm mất màu dung dịch có chứa 8g Br2 trong CCl4. Đem phần còn lại đi đốt cháy hoàn toàn thì thu được 17,6g khí CO2 (đktc) sinh ra. Tính phần trăm của mỗi chất có trong hỗn hợp X ban đầu.
Lời giải:
\begin{aligned}
&\text{Gọi }n_{C_2H_5OH}=x,\ n_{C_3H_5OH}=y,\ n_{C_3H_5OH}=z\\
&\text{Phần 1:}\\
&\bull C_2H_5OH +Na\to C_2H_5ONa+\frac{1}{2}H_2\\\
&\bull CH_3CH_2CH_2OH+Na\to CH_3CH_2CH_2ONa+\frac{1}{2}H_2\\\
&\bull CH_2=CH-CH_2-OH+Na\to CH_2=CH-CH_2-ONa+\frac{1}{2}H_2\ \\
&\text{Ta có: }n_{C_2H_5OH}+n_{C_3H_7OH}+n_{C_3H_5OH}=x+y+z=2n_{H_2}=2.0,075=0,15 (mol)\ (I)\\
&\text{Phần 2:}\\
&\bull CH_2=CH-CH_2-OH+Br_2\to CH_2Br-CHBr-CH_2OH\\
&\text{Ta có: }n_{C_3H_5OH}=z=n_{Br_2}=0,05 (mol)\\
&(I)\Leftrightarrow x+y=0,1.\\
&\text{Phần 3:}\\
&\bull C_2H_5OH+3O_2\to 2CO_2+3H_2O\\
&\bull C_3H_7OH+\frac{9}{2}O_2\to 3CO_2+4H_2O\\
&\bull C_3H_5OH+4O_2\to 3CO_2+3H_2O\\
&n_{CO_2}=2x+3y+3z=2x+3y+3.0,05=0,4\ (mol) \Leftrightarrow 2x+3y=0,25\\
&\text{Ta có hệ phương trình:}\begin{cases} x+y=0,1\\2x+3y=0,25\end{cases}
\Rightarrow x=y=0,05\ (mol)\\
&\text{Vậy, trong hỗn hợp X sẽ có: }\\
&m_{C_2H_5OH}=2,3\ (g);\ m_{C_3H_7OH}=3,0\ (g);\ m_{C_3H_5OH}=2,9\ (g).\\
&\text{Theo đó, ta sẽ tính được phần trăm khối lượng: }\\
&\%C_2H_5OH=28,05\%;\ \%C_3H_7OH=36,58\%;\ \%C_3H_5OH=35,37\%
\end{aligned}Bài 2: Cho ancol anlylic tác dụng với dung dịch HBr dư, đậm đặc thì sản phẩm chính thu được gồm những chất nào?
Lời giải: Với dung dịch HBr đậm đặc, dư thì sẽ xảy ra các phản ứng như sau:
CH_2=CH-CH_2-OH+HBr\to CH_2-CH-CH_2Br+H_2O
\\
CH_2-CH-CH_2Br+HBr\to CH_3-CHBr-CH_2Br
Bài 3: Hỗn hợp X gồm hex-1-in, axit acrylic, ancol anlylic. Cho khí hiđro đi qua a gam hỗn hợp X đun nóng (có chất xúc tác là Ni), sau một thời gian thu được (a+ 0,4) gam hỗn hợp Y gồm những hợp chất hữu cơ. Cho Y tác dụng với dung dịch Br2 dư thì có 0,25g Br2 cho phản ứng. Mặt khác, khi đốt cháy hoàn toàn a gam X rồi cho sản phẩm cháy vào nước vôi trong dư, thu được kết tủa có khối lượng là bao nhiêu?
Lời giải:
\begin{aligned}
&\text{Ta có: } n_{H_2} = \frac{0,4}{2} = 0,2 (mol).\\
&\text{Áp dụng bảo toàn liên kết pi, ta có:}\\
&2n_{C_6H_{10}} + n_{C_3H_4O_2} + n_{C_3H_6O} = n_{H_2}+ n_{Br_2} = 0,45\\
&n_{CO_2} = 6n_{C_6H_{10}} + 3n_{C_3H_4O_2} + 3n_{C_3H_6O} = 0,45.3 = 1,35\\
&Ca(OH)_2 \text{ dư nên ta suy ra }n_{CaCO_3} = 1,35.\\
&\text{Từ đó, khối lượng }CaCO_3 \text{ thu được sẽ bằng 135 gam.}
\end{aligned}Học online livestream Hóa 10 – 11 – 12 chất lượng, uy tín tại Marathon Education
Kiến thức về Ancol Anlylic không quá phức tạp. Tuy nhiên, ancol này rất hay xuất hiện trong các đề kiểm tra. Vì thế, các em nên dành nhiều thời gian ôn luyện và làm quen với các dạng bài tập. Các em có thể tham khảo khóa học online livestream tại Marathon Education. Được biết đến là một nền tảng học trực tuyến Toán – Lý – Hóa THPT uy tín và chất lượng, Marathon Education là “người bạn đồng hành” của nhiều thế hệ học sinh.
Ở Marathon Education, các em sẽ được giảng dạy bởi những thầy cô thuộc TOP 1% các giáo viên dạy giỏi toàn quốc. Không những vậy, nếu quá trình học có xảy ra vấn đề gì, các em sẽ được hỗ trợ kịp thời bởi đội ngũ cố vấn học tập chuyên môn.
Ngoài ra, để thời gian học tập luôn được suôn sẻ, không gián đoạn, những yếu tố như đường truyền, âm thanh và hình ảnh được team Marathon Education đảm bảo rõ nét, chân thực và sống động. Các lớp học online tại đây còn được mô phỏng giống hệt một lớp học offline bình thường. Điều này sẽ giúp tăng sự tương tác giữa thầy cô và học sinh.
Khi trở thành học viên tại Marathon Education, các em sẽ được nhận ngay cuốn sổ tay học tập Toán – Lý – Hóa được biên soạn tỉ mỉ và chi tiết. Tài liệu này sẽ hỗ trợ cho việc ôn luyện và củng cố kiến thức của các em.
Nếu cảm thấy hứng thú với các lớp học online tại Marathon Education, hãy nhanh tay đăng ký học livestream tại Marathon Education ngay hôm nay để nhận được khuyến mãi học phí các khóa học lên đến 39%, từ 699K chỉ còn 399K.
Công thức, tính chất và các bài tập về Ancol Anlylic là kiến thức các em cần phải ghi nhớ. Hy vọng thông qua bài viết, các em sẽ khám phá thêm được nhiều điều mới mẻ và bổ ích. Chúc các em có những buổi học thật hiệu quả và đạt được thành tích cao trong học tập.